 |
Класифікація та номенклатура ферментів
Дата добавления: 2014-07-26 | Просмотров: 1631
|
|
Кожен фермент має дві назви. Перша – коротка, так звана робоча, зручна для повсякденного користування. Друга (більш повна) – систематична, що використовується для однозначної ідентифікації ферменту.
У назві більшості ферментів міститься суфікс «аза», приєднаний до назви субстрату реакції, наприклад, уреаза, сахараза, ліпаза, нуклеаза або до назви хімічного перетворення певного субстрату, наприклад, лактатдегідрогеназа, аденілатциклаза, фосфоглюкомутаза, піруваткарбокси-лаза. Згідно українській класифікації ферментів (КФ), назви ферментів пишуться разом. Але у вжитку зберігся ряд тривіальних, історично закріплених назв ферментів, які не дають уявлення ні про субстрат, ні про тип хімічного перетворення, наприклад трипсин, пепсин, ренін, тромбін.
Міжнародний союз біохімії і молекулярної біології у 1961 р. розробив систематичну номенклатуру, згідно якої усі ферменти розбиті на 6 основних класів у залежності від типу хімічної реакції, яку вони каталізують. Кожен клас складається з чисельних підкласів і підпідкласів з урахуванням перетворюваної хімічної групи субстрату, донора та акцептора перетворюваних груп, наявність додаткових молекул і т.д. Кожен з 6-ти класів має свій порядковий номер, чітко за ним закріплений.
Перший клас ферментів "Оксидоредуктази" каталізують різні окисно-відновні реакції за участю двох субстратів (перенесення електронів або атомів водню з одного субстрату на інший). Систематичну назву ферментів складають за формулою «донор: акцептор – оксидоредуктаза», робочу – субстрат–підклас оксидо-редуктаз.
До підкласу дегідрогенази входять ферменти, що каталізують реакції дегідрування (відщеплення водню). В якості акцепторів водню використовуються коферменти NAD+, NADP+, FAD, FMN (див. нижче). Усі ферменти цієї групи володіють високою субстратною специфічністю. Приклад реакції:

Ферменти, що відносяться до підкласу оксидази каталізують реакції, в яких акцептором електрону служить молекулярний кисень. Приклад реакції, що каталізується цитохромоксидазою:

Оксигенази (гідроксилази) – каталізують реакції перенесення на субстрат атому оксигену з молекули кисню на субстрат. Приклад реакції:

Другий клас ферментів "Трансферази" каталізують реакції перенесення функціональних груп від однієї сполуки до іншої. Їх класифікують в залежності від групи, що переноситься. Назву цих ферментів складають за формулою «донор:акцептор – транспортована група – трансфераза». До класу трансфераз належать амінотрансферази, ацилтрансферази, метилтрансферази, глікозилтрансферази, кінази (фосфотрансферази). Приклади реакції:

Третій клас ферментів "Гідролази" каталізують реакції гідролізу (розщеплення ковалентного зв’язку з приєднанням молекули води по місцю розриву). Розділяють на підкласи в залежності від зв’язку, що розщеплюється. Назва ферментів складається за формулою «субстрат–гідролаза» або прямим приєднанням до назви субстрату суфіксу «аза», наприклад протеаза, ліпаза, фосфоліпаза, рибонуклеаза. Приклад реакції:

Для окремих класів гідролаз використовують спеціальні терміни, що характеризують гідроліз певного хімічного зв’язку: естерази, фосфатази та ін.
Четвертий клас ферментів "Ліази" відщеплюють від субстратів негідролітичним шляхом певну групу (при цьому можуть відщеплюватися СО2, Н2О, NH2, SH2 та ін.) або приєднують молекулу води (найчастіше) по подвійному зв’язку. Назви ферментів складаються за формулою «субстрат–група, що приєднується або відщеплюється». Приклади реакцій:
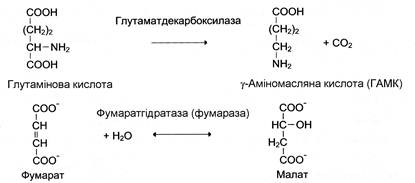
П'ятий клас ферментів "Ізомерази" каталізують різноманітні внутрішньомолекулярні перетворення. Їх класифікують у залежності від типу реакції ізомеризації. Як загальну назву ферментів цього класу використовують термін «ізомерази», наприклад:

Ізомерази можуть каталізувати внутрішньомолекулярні окисно-віднов-ні реакції, здійснюючи взаємоперетворення альдоз і кетоз, кетонних і енольних груп, переміщення подвійних зв’язків всередині молекули:
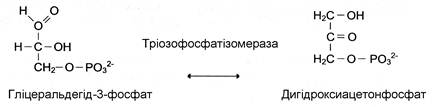
Коли ізомеризація полягає у внутрішньомолекулярному перенесенні групи, фермент називають мутазою, наприклад:

Шостий клас ферментів "Лігази" (синтетази) Каталізують реакції приєднання двох молекул одна до одної з утворенням ковалентного зв’язку. Цей процес спряжений з розривом фосфоефірного зв’язку у молекулі АТФ (або інших нуклеозидтрифосфатів) або з розривом макроергічних зв’язків інших сполук. У першому випадку (при використанні енергії гідролізу АТФ) такі ферменти називають лігазами або синтетазами:

У випадку, коли джерелом енергії слугує будь-яка інша макроергічна сполука (не АТФ), ферменти називають синтазами:
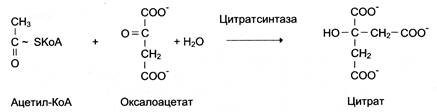
У відповідності з класифікацією кожен фермент має систематичну назву, що однозначно характеризує хімічну реакцію, яку він каталізує. Наприклад, субстрат D-гліцеральдегід-3-фосфат: фермент NAD–оксидоредуктаза (робоча назва – гліцеральдегідфосфат дегідрогеназа). З назви ферменту випливає, що субстратом цього ферменту є D-гліцеральдегід-3-фосфат, тип каталізованої реакції – окисно-відновна в присутності коферменту NAD+.
У 1972 р. комісією з номенклатури біохімічних сполук Міжнародного союзу теоретичної та прикладної хімії були запропоновані «Правила номенклатури ферментів», що мають кодове чотиризначне цифрове позначення, де перша цифра означає клас ферменту, друга цифра (підклас) уточнює, яка група перетворюється, третя (підпідклас) уточнює додаткових учасників реакції (наприклад, донора і акцептора) і четверта – порядковий номер ферменту у даній підгрупі. Так, фермент малатдегідрогеназа має систематичну назву L-малат: NAD–оксидоредуктаза і має кодовий шифр 1.1.1.38. Шифр означає, що цей фермент належить до першого класу ферментів – оксидоредуктаз, окислювана група – гідроксильне угрупування (1) у присутності коферменту NAD+ (1) і порядковий номер ферменту у цій підгрупі – 38. Кодову номенклатуру ферментів в основному використовують в науковій літературі.