 |
Молекулярна маса ВМС
Дата добавления: 2014-10-03 | Просмотров: 1826
|
|
Одним із найважливіших параметрів ВМС є молекулярна маса. Як правило, ВМС складаються із суміші макромолекул з різними молекулярними масами. Тому для її характеристики використовують середні значення молекулярної маси: це середньочисельна Мn і середньомасова Мm молекулярні маси.
Середньочисельна молекулярна маса показує середню масу, що припадає на одну частинку:
Mn = Sni∙Mi/Sni ( 10.4)
де ni- кількість макромолекул з молярною масою М.
Середньомасова молекулярна маса показує відношення маси даної фракції до загальної маси ВМС:
Mn = Smi∙Mi/Smi ( 10.5)
де m- маса молекул з молярною масою M.
Якщо ВМС має макромолекули одного розміру, то Мm = Мn.
В інших випадках Мm>Мn, а їх співвідношення називається коефіцієнтом дисперсності.
Методи визначення молекулярної маси ВМС поділяються на:
Хімічні – пов’язані з визначенням кількості функціональних груп.
Термодинамічні – зводяться до визначення мольної частки ВМС в розчині.
Молекулярно – кінетичні методи основані на явищах дифузії, ультрацентрифугування, та визначені в’язкості.
Оптичні – основані на визначенні інтенсивності розсіювання світла.
Віскозиметричні – основані на вимірювання в’язкості розчину ВМС.
Розглянемо віскозиметричний метод визначення молекулярної маси ВМС. В’язкість розчинів ВМС набагато вища, ніж розчинів низькомолекулярних сполук з такою самою об’ємною концентрацією. Експериментальні дані показали, що питома в’язкість зростає з ростом молекулярної маси при сталих концентраціях.
Штаудінгер запропонував залежність в’язкості розчину ВМС лінійної структури від молекулярної маси полімеру:
hпит = К∙М∙с ( 10.6)
де hпит - питома в’язкість;
К - стала гомологічного ряду полімерів.
hпит = (h - hо)/hо ( 10.7)
де h, hо - відповідно, в’язкості розчину та розчинника.
Питома в’язкість, віднесена до концентрації системи, називається зведеною в’язкістю
hзв =hпит/с =КМ ( 10.8)
Для розчинів ВМС зведена в’язкість hзв зростає із збільшенням концентрації. Це зростання зумовлене підсиленням взаємодії між макромолекулами. Екстраполюючи залежність в’язкості від концентрації (рис. 74) на вісь ординат, одержуємо характеристичну в’язкість:
[h] = lim (hпит/c) ( 10.9)
Характеристична в’язкість не залежить від концентрації розчину та конформаційного стану макромолекул. Залежність характеристичної в’язкості від молекулярної маси описується рівнянням Марка-Куна - Хаувінка:
[h] = k∙Мa ( 10.10)
де k- стала для гомологічного ряду полімерів.
a - параметр, що характеризує форму макромолекули в розчині.
Його значення змінюється в межах 0,55-0,85 та характеризує пружність ланцюгів макромолекули в розчині.

Рис. 74. Визначення характеристичної в’язкості розчину ВМС.
Коефіцієнти k і a визначають експериментально. За даними характеристичної в’язкості можна розрахувати середню молекулярну масу ВМС.
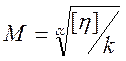 ( 10.11)
( 10.11)
Приклад 10.1
Зразок синтетичного каучуку масою 0,17564 кг помістили в бензол. Через 24 години витримки при 25 °С маса цього зразка стала рівною 0,53921 кг Розрахуйте ступінь набухання зразка каучука в бензолі за вказаних умов.
a = (0,53921 - 0,17564)/0,17564= 2,07 = 207 %.
Приклад 10.2
Характеристична в'язкість розчину зразка синтетичного каучуку в толуолі при 20 °С дорівнює 4,62∙10-3 м3/моль. Розрахуйте середню молярну масу цього каучуку в умовах випробування. Сталі k і a рівняння Марка Куна Хаувінка прийняти рівними 5,14∙10-5 моль/м3 і 0,67.
 кг/моль
кг/моль
Контрольні питання
1. Які властивості характерні ВМС? Як вони залежать від структури ВМС?
2. Як утворюються дисперсії полімерів? Наведіть приклади, охарактеризуйте їхні оптичні властивості.
3. Який процес називають набряканням? Що таке ступінь набрякання?
4. На які стадії можна полити процес набрякання?
5. Що таке тиск набрякання? Як його можна розрахувати?
6. .Які системи називаються драглями. Наведіть приклади обмеженого і необмеженого набрякання драглів. Як впливає температура на процес набрякання драглів?
7. У чому проявляється старіння колоїдних систем? Що таке синерезис?
8. Що таке застигання полімерів? Які фактори сприяють застиганню?
9. Що таке середньочисельна та середньомасова молекулярні маси полімеру?
10. Охарактеризуйте властивості і практичне значення високомолекулярних іонітів. Наведіть приклади катіонітів і аніонітів.
11. Назвіть особливості поводження амфотерних високомолекулярних поліелектролітів у розчинах. Наведіть визначення ізоелектричного стану.
12. Наведіть способи визначення молекулярної маси полімерів.
13. Віскозиметричний метод визначення молекулярної маси ВМС. Рівняння Марка-Куна-Хаувінка.